Minimal invasive Darmresektion oder die Chirurgie des Morbus Hirschsprung im Wandel der Zeit
Zum Thema Morbus Hirschsprung:
Der, 1886 erstmalig beschriebene, so genannte Morbus Hirschsprung ist eine typische und seltene chirurgische Erkrankung des Kindesalters (1: 5000 Geburten), bei der eine schwere nervale Motilitätstörung (1846 Ehrenpreis), des Dickdarms bis zum After, vorliegt. Im erkrankten Darmsegment fehlen die Ganglienzellen, es ist enggestellt und effektive, propulsive – also den Stuhl vorantreibende - peristaltische Wellen fehlen. Üblicherweise, d.h. in etwa 60%, betrifft der M. Hirschsprung das Enddarmabschnitt (Rectosigmoid), kann aber in einerseits als sogenannte „kurze Form“ nur distale Mastdarmanteile (Rectum) oder als „lange Form“ auch das gesamte Colon betreffen.
Ein weiters wichtiges Kennzeichen des Krankheitsbildes ist die lebenslange Verkrampfung (Engstellung) des Afters (Analkanals), bezeichnet als sogenannte „Analsphinkterachalasie“.

Abb. 1: Häufigkeitsverteilung der betroffenen Dikadarmabschnitte
Die Hirschsprung-Krankheit geht mit komplexen genetischen Veränderungen einher, wobei mehrere Genmutationen als krankheitsassoziiert nachgewiesen wurden. Das wichtigste identifizierte Gen mit einer Mutation ist das RET-Gen. Darüber hinaus scheinen weitere Mutationen in mindestens 6 verschiedenen Genen von Bedeutung zu sein. Die Genetik des Morbus Hirschsprung ist so komplex, dass das Vorhandensein einer bekannten krankheitsverursachenden Mutation nicht unbedingt zu einem Auftreten des Morbus Hirschsprung führt. Nicht alle Mutationsträger entwickeln die Krankheit. 90 % der Hirschsprung-Krankheit tritt als isolierte Erkrankung auf. 7-10 % der Patienten haben bereits einen anderen Fall in der Familie. Vorbeugende Maßnahmen zur Verhinderung dieser Krankheit sind bisher nicht bekannt. In etwa 5-12% der Patienten finden sich Begleitmissbildungen, wobei die Trisomie 21 und Herzfehler an erster Stelle zu nennen sind.
Zur Klinik:
Im Vordergrund steht eine, von Geburt an bestehende Obstipation mit erheblicher Passagestörung und verzögertem Mekoniumabgang (Neugeborenenstuhl) innerhalb der ersten 48 Lebensstunden. Möglicherweise lebensgefährliche Beschwerden des Darmverschlusses (Subileus-, bzw. Ileussymptomatik) steht im Vordergrund. Beim Setzen eines weichen Darmrohres, wo der verkrampfte enge Darm überbrückt wird, entleeren sich „explosionsartig“ Gase und Stuhl. Der unvorbereitete diagnostische Röngen – Kontrastmittel – Einlauf (Irrigoskopie) zeigt ein typisches Bild mit engestelltem Endarm und dem typischen Konus, der über eine Übergangszone in den gesunden, also regulär mit Ganglienzellen bestückten Darm mündet.
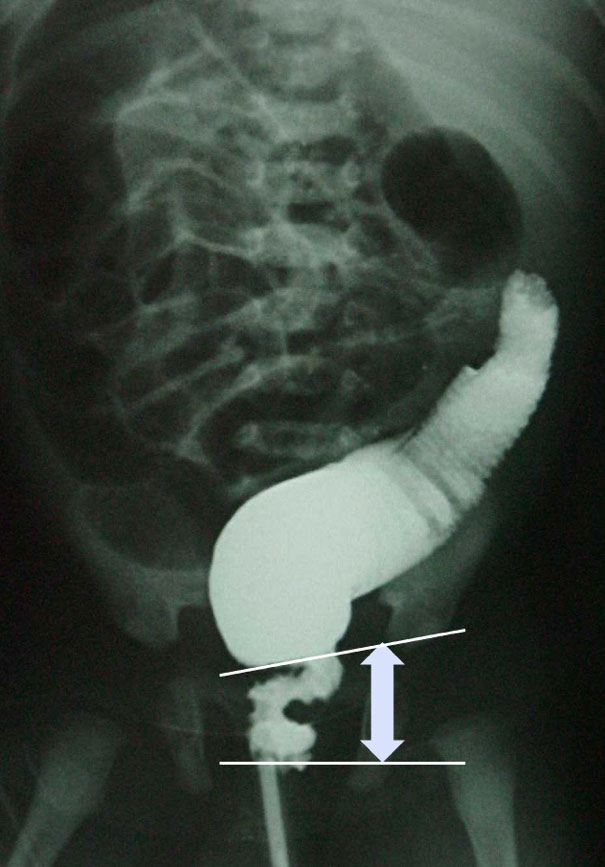
Abb. 2: Kontrastmitteldarstellung (Irrigoskopie) des engen, nicht Stuhl befördernden Enddarms bei M. Hirschsprung
Der weitere Schritt in der Diagnostik sind kleinste Gewebeproben (Biopsien) aus den vermeintlich betroffenen Darmabschnitten. Oftmals genügen Probeentnahmen aus dem Enddarm. Beweisend sind bioptisch fehlende Ganglienzellen und eine sogenannte cholinerge Nervenfaserhypertrophie (Acetylcholinfaserfärbug in der entnommenen Gewebeprobe) sowie der oftmals nachweisbare fehlender rectoanaler Erschlaffungsreflex in der analen Sphinktermanometrie (problematisch in der Aussage bei Neugeborenen). Auch eine Magnetresonanz (MRI) und eine analendosonographische Untersuchung können zusätzliche Informationen bringen. All diese Untersuchungen sind in Betracht zu ziehen um die Problematik der Verstopfung (Obstipation) korrekt zu erfassen.
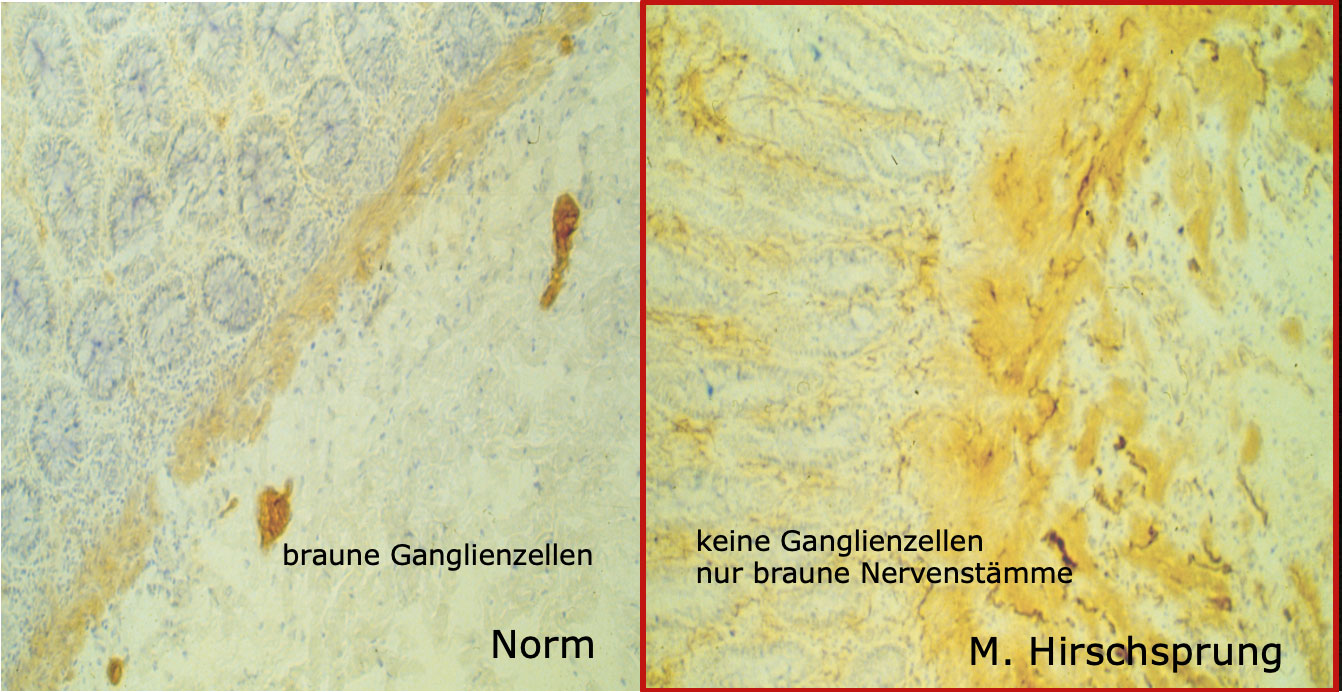
Abb. 3: Die Darmgewebeproben werden mit der Acetylcholinesterasereaktion gefärbt und man erkennt im gesunden Darm braune Ganglienzellen und im erkrankten M. Hirschsprung-Darm (rot umrandet) nur verdichte braune Nervengeflechte
Die Hirschsprung´sche Erkrankung ist, u.a. durch den Stuhlstau, von einer signifikant erhöhten Inzidenz an schwersten, lebensgefährlichen Darminfektionen (Enterokolitiden 12% - 58%) begleitet. Im Rahmen dieser Enterokolitis kann es zur Entwicklung eines so genannten „toxischen Megacolons“ (Weitstellung und Lähmung des Dickdarmes durch eine entzündliche Reaktion) kommen. Krankmachende Keime im Stuhl sind (Clostridium difficile, Staphylokokkus aureus, Anaerobier), die durch den stehengebliebenen Stuhl im Darmtrakt wuchern. Der überdehnte Darm ist durchblutungsgefährdet und die Keimbarriere zur Blutbahn wird geschwächt. Es resultiert hohes Fieber und eine lebensgefährliche Blutvergiftung.
Therapie und Operationstechniken:
Für die rekonstruktive Chirurgie am rektoanalen Bereich sind entsprechend der AWMF-Leitlinien folgende wichtige präoperativen Untersuchungen empfohlen (Kontrastmitteldarstellung, Analmanometrie, Druckmessung/Analmanometrie, Gewebeprobenentnahme mit Histologie und Histochemie). Ergänzend hat die Elektrostimulation in Narkose (Keine lähmende Lokalanästhesie!) und die Analendosonografie zur Beurteilung des Schließmuskelapparates aus medizinischer und wissenschaftlicher Sicht ihre Bedeutung.
Mit dem Ziel, eine lebensnotwendige ausreichende Darmentleerung rasch herzustellen, ergeben sich folgende prinzipielle therapeutische Ansatzpunkte[1]:
- Darmspülungen und Entleerungen über regelmäßig applizierte Darmrohre. Dadurch wird gestauter Stuhl entleert und einer Überdehnung des Darmes entgegenbewirkt.
- Primäres Anlegen eines vorübergehenden künstlichen Darmausganges (Enterostomie bzw. Colostomie). Diese kann entweder weit oberhalb, beispielsweise im Bereich der linken Colonflexur oder als so genannte „leveling“ Colostomie am Übergangssegment vom ganglionärem zum aganglionärem Darm gewählt werden (favorisiertes Verfahren). Die proximale Ausleitung hat den Grund die spätere abdominoperineale Resektion nicht zu behindern. Die „leveling“ Colostomie wird m Rahmen der Resektion, im Alter von etwa 2 – 5 Monaten, aufgelöst (zweizeitiges Verfahren).
- Die möglichst radikale Resektion des aganglionären Darmanteiles mit dem Ziel der Herstellung einer normalen Stuhlpassage (Defäkation), der Vermeidung einer weiterhin problematischen Verstopfung (Enterokolitis; wiederkehrender Morbus Hirschsprung) durch ebenfalls bestehenden Schließmuskelkrampf (Sphinkterachalasie) und andererseits die Kontinenzfunktion des Analkanls möglichst optimal beizubehalten. Wenn im Rahmen der Darmresektion einen Stumpf des erkrankten, nicht funktionierenden, Darmes belassen wird, so wird dieser im Zuge des Wachstums länger und die Morbus Hirschsprung – Probleme sind wieder da.
Seit den 50iger Jahren eine Reihe von Resektionsverfahren entwickelt, um oben genannten Aspekten gerecht zu werden. Die Maxime der chirurgischen Therapie ist die Entfernung des erkrankten Darmsegmentes und die Herstellung eines weitgehend normalen Defäkationsmusters.
- 1948/1950 beschrieb erstmals Swenson und später von Grob modifiziert, eine „pull through“ Technik der abdominoperinealen Resektion, bei der erkrankte Darm in seinem extraperitonealen Verlauf so weit wie möglich präpariert, transanal eventriert und anschließend reseziert wurde [2].
- 1956/1962 stellten Duhamel und Martin die Technik der Resektion mit retrorektalem transanalem Durchzug vor. Dabei bleibt an der vorderen Rektumzirkumferenz, sozusagen semizirkulär, aganglionärer Darm stehen. Obwohl diese Methode bei Rezidiveingriffen auch heute Verwendung findet, so wurde sie im angloamerikanischen Raum primär nur zu 30% eingesetzt. Probleme ergaben sich aus dem belassenen „blind pouch“ ausgehend vom vorderen aganglionären Darmanteil [3].
- Im deutschen Sprachraum etablierte sich über viele Jahre die tiefe vordere Resektion nach Rehbein und State. Dabei wird ein aganglionärer Restcolonanteil in einer Länge zwischen 3 und 5cm belassen. Damit entspricht diese Resektion einer tiefen vorderen Resektion mit Eröffnung der peritonealen Umschlagsfalte im Douglasbereich [4]. Unvorteilhafte Resultate, im Sinne eines Rezidivmegacolons, ergaben sich hauptsächlich aus dem Umstand, dass man die, im Therapiekonzept inkludierten, kräftigen Dilatationen des Analkanales und die, in bestimmten Fällen, angegebene Sphinkterotomie (wegen der Sphinkterachalasie) nicht strikt junktimiert zum Verfahren eingehalten hat. In den Fällen eines sekundären Megakolons infolge eines „zu langen“ belassenen aganglionären Segmentes führen wir eine Nachresektion mit abdomino-perinealem Durchzug und coloanaler Anastomose durch.
- 1964 wurde der intrasphinktäre transanale Durchzug nach Soave, später modifiziert vonBoley vorgestellt [5, 6]. Hier wird im Sinne einer „pull through“ Methode nach endorectaler Dissektion des Mucosaschlauches, regulär innervierter Darm mit dem Analkanal verbunden. Der Anschluss erfolgt oberhalb des sogenannten unverhornt epithelialisierten sensiblen äußeren Analhaut (Anoderm). Dabei wird die Anatomose, je nach Einschätzung des Chirurgen, unterschiedlich hoch oberhalb des sogenannten gezahnten Übergangs zwischen Darmschleimhaut und Analhaut (Linea dentata) in verschiedenen Höhen angelegt. Erfahrungsgemäß halte ich erfahrungsgemäß das Ziel nahe bzw. knapp an der Linea dentata den gesunden Darm anzuschließen für vorteilhaft, weil das Komplikationsrisiko eine Enterokolitis mit an Sicherheit grenzender Wahrscheinlichkeit wegfällt.
Es gilt, wie gesagt, den lebenslang bestehenden Schließmuskelkrampf (Sphinkterachalasie [7, 8]) mit Hilfe des unmittelbar nahen gesunden Darms zu überwinden. Sollte die Anastomose nur „wenige Millimeter“ zu hoch angelegt sein, so wird der nachfolgenden Passage-Störung durch den Sphinkterkrampf durch Botulinum – Toxin Injektionen, oder die Durchtrennung des inneren Schließmuskels (Sphinkterotomie) begegnet [9-12].
Stenoseprobleme ergaben sich auch durch das bestehen lassen eines zu langen den durchgezogenen gesunden Darm umhüllenden muskulären, aganglionären Rectumschlauches (Rollkrageneffekt). Heute wird, in einer weiteren Modifikation, die Spaltung desselben bis oberhalb der Puborectalisschlinge vorgenommen. Mit dieser sinnvollen technischen Ergänzung hat das Verfahren des intrasphinktären transanalen Durchzugs in den letzten Jahren eine Renaissance erfahren, sich bis heute durchgesetzt und darüber hinaus in einer weiterentwickelten OP – Technik (siehe 5.) neuerlich große Aktualität erlangt. Der offene abdomioperineale Durchzug nach Soave/Boley mit coloanaler Anastomose ist das gängige Standardverfahren bei langstreckigen Formen der Aganglionose. Schon 1979 publizierte Kleinhaus, dass die Soave/Boley Technik mit einer Mehrheit von etwa 50% zur Anwendung gebracht wird[13].
- 1998 wurde, dem Prinzip von Soave/Boley folgend, der transanale endorectale Durchzug von De la Torre vorgestellt[14] Bei diesem Resektionsverfahren wird keine Laparotomie durchgeführt. Der Analkanal wir vorsichtig dilatiert und anschließend mit Haltenähten aufgespannt. Wir verwenden dazu eine Colostomieplatte. Knapp oberhalb der Linea dentata erfolgt die zirkuläre Inzision und Dissektion des Muscosaschlauches. In einer Höhe von etwa 6-7 cm wird ventral der muskuläre Rectummantel inzidiert und damit der Douglas eröffnet. Nach zirkulärer Durchtrennung der Rectummuskulatur erfolgt die weitere transanale Mobilisierung, wobei die mesosigmoidalen Gefäße darmwandnahe unterfahren, koaguliert und durchtrennt werden. Mit dieser transanalen Dissektion können distale, aganglionäre, rectosigmoidale Darmanteile bis zu einer Länge von rund 20 cm problemlos mobilisiert und schließlich reseziert werden. Nach Erreichen des konischen Übergangssegmentes ergibt die Gefrierschnittsuntersuchung den Hinweis, ob bereits genügend Ganglienzellen vorliegen. Nach Absetzen des Präparates erfolgt die coloanale Anastomose. Sollte die Aganglionose ein längeres Colonsegment betreffen so erfolgt mittels Laparotomie der Umstieg zur konventionellen Durchzugsoperation nach Soave/Boley. Diese Vorgangsweise sollte eingehalten werden, nachdem bei langstreckigen transanalen Mobilisationen, zum Beispiel bei atypisch langem aganglionärem Segment, öfters postoperative Komplikationen zu erwarten sind.
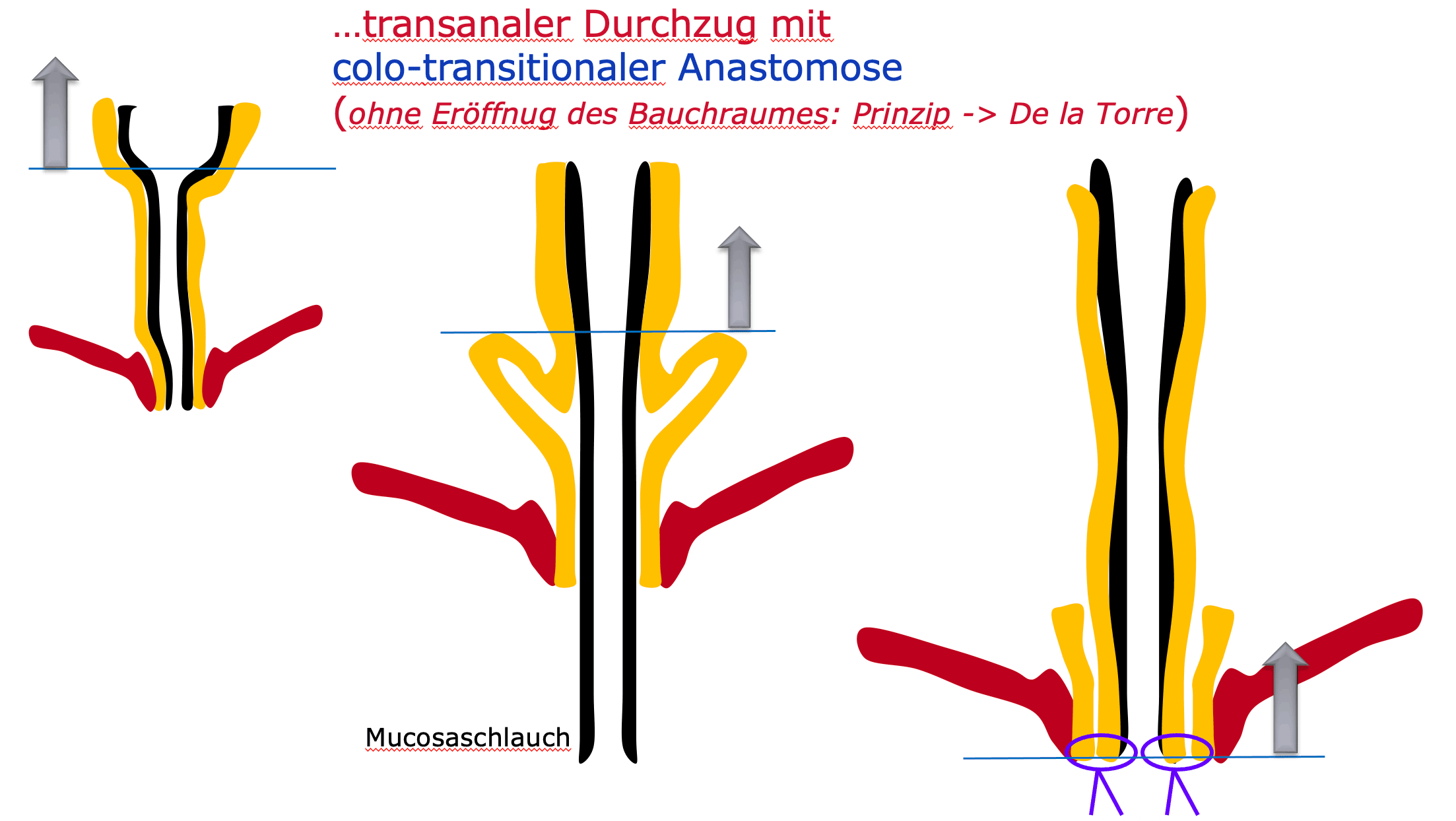
Abb. 4: transanaler Durchzug mit mit colo-transitionaler Anastomose (ohne Eröffnung des Bauchraumes: Prinzip -> De la Torre)
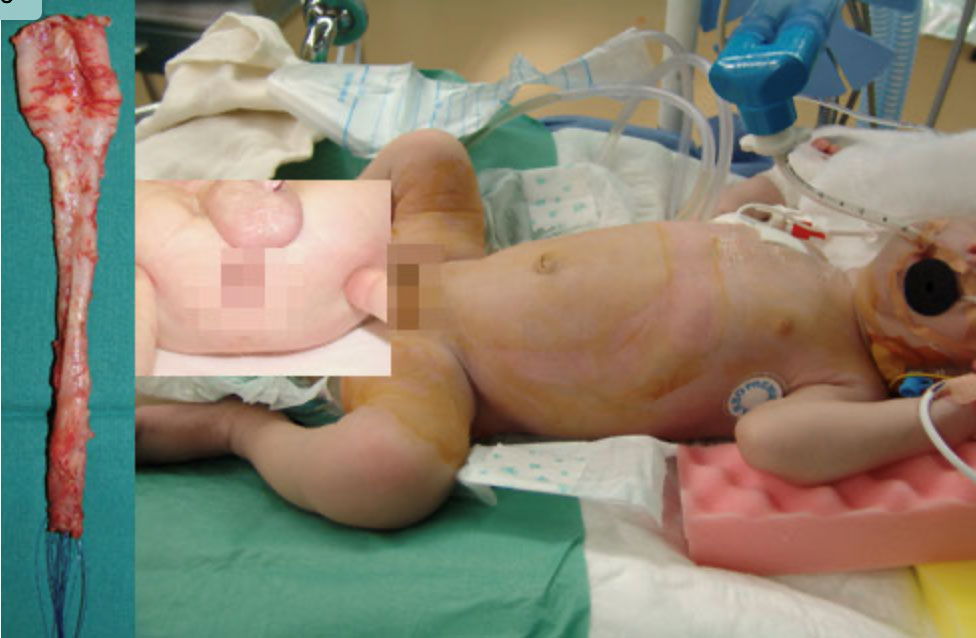
Abb. 5: Entfernter Darm und postoperatives Bild von einem 1Mo. alten Patienten, wo der erkrankte Darm durch den After entfernt wurde, ohne den Bauchraum zu eröffnen
Drei-, zwei- und einzeitige Korrektur:
Die chirurgische Behandlung des Morbus Hirschsprung bestand üblicherweise aus einem mehrzeitigen Vorgehen. Primär wurde zur Darmentlastung eine Enterostomie (proximal oder „leveling“) angelegt, um nach einem Intervall von etwa 3 bis 5 Monaten die Resektion vorzunehmen. Proximale Enterostomien, die dann als so genannte Schutzenterostomien fungierten, wurden später nach Abheilung der coloanalen Anastomose gesondert geschlossen. Die „leveling“ Colostomie werden im Rahmen der abdominoperinealen Resektion aufgelöst.
In den letzten 10 Jahren entwickelte sich, unter Zugrundelegung des Resektionsverfahrens von Soave/Boley, der Trend zur primären und einzeitigen Korrektur bereits im Neugeborenenalter. Natürlich gibt es, nach wie vor, colostomiepflichtige Fälle, in denen auch durch wiederholte Darmspülungen keine adäquate Entleerung herbeigeführt werden kann und die Darmverschluss-Symptomatik andauernd vorhanden bleibt
Die eingesetzten Operationsverfahren haben sich im Laufe der Zeit gewandelt. Haben wir 1995 alle Patienten noch nach der State/Rehbein Resektionstechnik versorgt so haben wir heute in allen Fällen den intrasphinktären - koloanalen Durchzug und diesen - ausschließlich mit transanalem Zugang ohne Eröffnung des Bauchraumes - bei etwa 50% der Patientenzur Anwendung bringen können.
Literatur:
- Langer JC: Hirschsprung disease. Curr Opin Pediatr 2013, 25(3):368-374.
- Swenson O, Bill AH, Jr.: Resection of rectum and rectosigmoid with preservation of the sphincter for benign spastic lesions producing megacolon; an experimental study. Surgery 1948, 24(2):212-220.
- Duhamel B: [New operation for congenital megacolon: retrorectal and transanal lowering of the colon, and its possible application to the treatment of various other malformations]. Presse Med (1893) 1956, 64(95):2249-2250.
- Rehbein F: [Operative therapy of Hirschsprung's disease]. Langenbecks Arch Klin Chir Ver Dtsch Z Chir 1953, 276:540-543.
- Soave F: A New Surgical Technique for Treatment of Hirschsprung's Disease. Surgery 1964, 56:1007-1014.
- Boley SJ: New Modification of the Surgical Treatment of Hirschsprung's Disease. Surgery 1964, 56:1015-1017.
- Langer JC, Rollins MD, Levitt M, Gosain A, Torre L, Kapur RP, Cowles RA, Horton J, Rothstein DH, Goldstein AM et al: Guidelines for the management of postoperative obstructive symptoms in children with Hirschsprung disease. Pediatr Surg Int 2017, 33(5):523-526.
- Gause CD, Krishnaswami S: Management of Anorectal Malformations and Hirschsprung Disease. Surg Clin North Am 2022, 102(5):695-714.
- Friedmacher F, Puri P: Comparison of posterior internal anal sphincter myectomy and intrasphincteric botulinum toxin injection for treatment of internal anal sphincter achalasia: a meta-analysis. Pediatr Surg Int 2012, 28(8):765-771.
- Wester T, Granstrom AL: Botulinum toxin is efficient to treat obstructive symptoms in children with Hirschsprung disease. Pediatr Surg Int 2015, 31(3):255-259.
- Pini Prato A, Faticato MG, Mazzola C, Arrigo S, Mattioli G, Arnoldi R, Mosconi M: Intrasphincteric BoTox injections in Hirschsprung's disease: indications and outcome in 64 procedures over a ten-year period. Minerva Pediatr 2018.
- Church JT, Gadepalli SK, Talishinsky T, Teitelbaum DH, Jarboe MD: Ultrasound-guided intrasphincteric botulinum toxin injection relieves obstructive defecation due to Hirschsprung's disease and internal anal sphincter achalasia. J Pediatr Surg 2017, 52(1):74-78.
- Kleinhaus S, Boley SJ, Sheran M, Sieber WK: Hirschsprung's disease -- a survey of the members of the Surgical Section of the American Academy of Pediatrics. J Pediatr Surg 1979, 14(5):588-597.
- De la Torre-Mondragon L, Ortega-Salgado JA: Transanal endorectal pull-through for Hirschsprung's disease. J Pediatr Surg 1998, 33(8):1283-1286.







